Bạn đã bao giờ thắc mắc “Thành phần chính của cồn là gì?” chưa? Khi nhắc đến “cồn”, có lẽ điều đầu tiên hiện lên trong đầu bạn là những ly bia mát lạnh, những chén rượu nồng ấm trong các buổi聚会, hoặc thậm chí là cồn sát khuẩn quen thuộc trong tủ thuốc gia đình. Nhưng liệu bạn đã thực sự hiểu rõ về “linh hồn” đứng sau những thức uống và sản phẩm quen thuộc này?
Trong bài viết hôm nay, chúng ta sẽ cùng nhau khám phá tất tần tật về thành phần chính của cồn. Từ định nghĩa khoa học, công thức hóa học đơn giản, những tính chất vật lý và hóa học đặc trưng, đến quá trình sản xuất cồn và ứng dụng đa dạng của nó trong đời sống. Hãy cùng nhau “bóc tách” và tìm hiểu sâu hơn về thành phần thú vị này nhé!
Thành phần chính của cồn là gì? “Ethanol” – Cái tên quen mà lạ
Để bắt đầu hành trình khám phá về cồn, chúng ta hãy cùng nhau tìm hiểu thành phần chính tạo nên “cồn” mà chúng ta thường nhắc đến hàng ngày. Câu trả lời chính là Ethanol.
Ethanol, còn được gọi là rượu etylic, là một hợp chất hóa học hữu cơ, thuộc nhóm alcohol. Đây chính là thành phần chính tạo nên tính chất đặc trưng của các loại đồ uống có cồn như bia, rượu, whisky, vodka… Ethanol cũng là thành phần quan trọng trong nhiều sản phẩm khác như cồn sát khuẩn, nhiên liệu sinh học, và dung môi công nghiệp.
Vậy, Ethanol có công thức hóa học và những đặc tính gì đặc biệt? Chúng ta hãy cùng nhau tìm hiểu sâu hơn nhé!
1. Công thức hóa học đơn giản nhưng “đa năng”
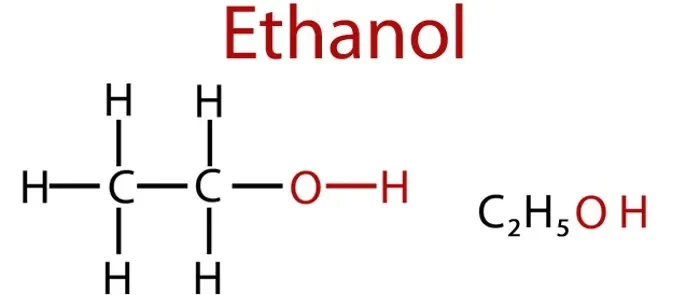
Ethanol có công thức hóa học là C₂H₅OH. Công thức này cho thấy, một phân tử Ethanol được cấu tạo từ:
- 2 nguyên tử Carbon (C)
- 6 nguyên tử Hydro (H)
- 1 nguyên tử Oxygen (O)
Sự kết hợp của các nguyên tử này tạo nên một cấu trúc phân tử đơn giản nhưng lại mang đến cho Ethanol những tính chất hóa học và vật lý vô cùng đặc trưng và “đa năng”.

2. Tính chất vật lý đặc trưng: Dễ bay hơi, dễ cháy, và “không màu, không mùi”
Ethanol sở hữu những tính chất vật lý rất dễ nhận biết và ứng dụng trong đời sống:
- Trạng thái: Ở điều kiện nhiệt độ và áp suất thông thường, Ethanol tồn tại ở trạng thái lỏng.
- Màu sắc và mùi: Ethanol nguyên chất là chất lỏng không màu và có mùi đặc trưng, thường được mô tả là mùi hơi hăng, cay nhẹ. Tuy nhiên, trong các sản phẩm như rượu bia, mùi của Ethanol thường bị “lấn át” bởi hương vị của các thành phần khác như hoa quả, ngũ cốc, hoặc gia vị.
- Độ bay hơi: Ethanol là chất lỏng dễ bay hơi, có nghĩa là nó dễ dàng chuyển từ trạng thái lỏng sang trạng thái khí ở nhiệt độ phòng. Tính chất này giúp Ethanol dễ dàng lan tỏa mùi hương và cũng là lý do vì sao cồn sát khuẩn bay hơi nhanh sau khi sử dụng.
- Tính dễ cháy: Ethanol là chất lỏng dễ cháy, khi cháy tạo ra ngọn lửa màu xanh lam và tỏa nhiệt. Tính chất này khiến Ethanol được sử dụng làm nhiên liệu trong một số ứng dụng.
- Hòa tan tốt trong nước và nhiều dung môi hữu cơ: Ethanol có khả năng hòa tan tốt trong nước và nhiều dung môi hữu cơ khác. Tính chất này giúp Ethanol được sử dụng làm dung môi trong nhiều ngành công nghiệp và sản xuất.

3. Tính chất hóa học nổi bật: Phản ứng đa dạng và khả năng hòa tan
Ethanol không chỉ có những tính chất vật lý đặc trưng, mà còn có những tính chất hóa học nổi bật, tạo nên sự “đa năng” của nó:
- Phản ứng cháy: Như đã đề cập ở trên, Ethanol dễ cháy và phản ứng với oxy trong không khí tạo ra khí CO₂ và nước, đồng thời giải phóng năng lượng lớn. Đây là phản ứng hóa học cơ bản và quan trọng nhất của Ethanol, được ứng dụng trong nhiên liệu và động cơ đốt trong.
- Phản ứng với kim loại kiềm: Ethanol phản ứng với các kim loại kiềm như Natri (Na) tạo ra muối ethoxide và khí Hydro (H₂). Phản ứng này thể hiện tính axit yếu của Ethanol.
- Phản ứng este hóa: Ethanol phản ứng với axit carboxylic tạo ra este và nước. Phản ứng este hóa được ứng dụng trong sản xuất hương liệu, mỹ phẩm, và dược phẩm. Ví dụ, este của Ethanol và axit axetic là ethyl acetate, một dung môi phổ biến và có mùi thơm dễ chịu.
- Phản ứng oxy hóa: Ethanol có thể bị oxy hóa thành aldehyde (acetaldehyde) và sau đó thành axit carboxylic (axetic acid). Phản ứng oxy hóa Ethanol trong cơ thể người là quá trình chuyển hóa cồn, tạo ra năng lượng nhưng cũng sinh ra các chất độc hại như acetaldehyde.
- Khả năng hòa tan: Ethanol là một dung môi phân cực, có khả năng hòa tan tốt cả các chất phân cực (như nước, muối) và các chất không phân cực (như dầu, chất béo). Tính chất này giúp Ethanol được sử dụng rộng rãi trong công nghiệp, mỹ phẩm, dược phẩm, và thực phẩm.
Quá trình sản xuất Ethanol: Từ tự nhiên đến công nghiệp
Vậy, Ethanol được sản xuất như thế nào? Có hai phương pháp sản xuất Ethanol chính: phương pháp sinh học (lên men) và phương pháp hóa học (tổng hợp hóa học).
1. Phương pháp sinh học (lên men): “Bí quyết” tạo ra đồ uống có cồn
Lên men là phương pháp sản xuất Ethanol cổ xưa nhất và vẫn được sử dụng rộng rãi cho đến ngày nay, đặc biệt là trong sản xuất đồ uống có cồn. Nguyên liệu chính để lên men Ethanol là các loại nguyên liệu chứa đường hoặc tinh bột, như:
- Ngũ cốc: Lúa mạch, lúa mì, ngô, gạo… (dùng trong sản xuất bia, whisky, vodka…)
- Hoa quả: Nho, táo, lê, mơ… (dùng trong sản xuất rượu vang, rượu táo…)
- Mía đường, củ cải đường, mật rỉ… (dùng trong sản xuất rượu rum, cồn công nghiệp…)
Quy trình lên men Ethanol cơ bản:
- Chuẩn bị nguyên liệu: Nguyên liệu được nghiền nhỏ, nấu chín (nếu là tinh bột) để chuyển hóa tinh bột thành đường.
- Lên men: Nguyên liệu đã chuẩn bị được trộn với men rượu (nấm men) trong điều kiện yếm khí (không có oxy). Men rượu sẽ “ăn” đường và chuyển hóa đường thành Ethanol và khí CO₂.
- Chưng cất (tùy chọn): Đối với các loại rượu mạnh, sau quá trình lên men, hỗn hợp được chưng cất để tăng nồng độ cồn. Bia thường không qua giai đoạn chưng cất, nên nồng độ cồn thấp hơn rượu.
- Lọc và tinh chế: Ethanol thô sau khi lên men hoặc chưng cất có thể được lọc và tinh chế để loại bỏ tạp chất và đạt được độ tinh khiết mong muốn.
2. Phương pháp hóa học (tổng hợp hóa học): Sản xuất cồn công nghiệp
Tổng hợp hóa học là phương pháp sản xuất Ethanol hiện đại, chủ yếu được sử dụng để sản xuất cồn công nghiệp. Phương pháp này dựa trên phản ứng hydrat hóa ethylene.
Phản ứng hydrat hóa ethylene:
- Nguyên liệu: Ethylene (C₂H₄), một sản phẩm của công nghiệp hóa dầu, và nước (H₂O).
- Điều kiện phản ứng: Xúc tác axit (thường là axit phosphoric), nhiệt độ cao (khoảng 300°C), và áp suất cao.
- Sản phẩm: Ethanol (C₂H₅OH).
Phương pháp tổng hợp hóa học cho phép sản xuất Ethanol với số lượng lớn, giá thành rẻ, và độ tinh khiết cao. Tuy nhiên, Ethanol sản xuất bằng phương pháp này thường được sử dụng trong công nghiệp, không dùng trong thực phẩm và đồ uống do có thể lẫn tạp chất.
Ứng dụng đa dạng của Ethanol: Không chỉ là đồ uống có cồn
Ethanol không chỉ là thành phần chính của đồ uống có cồn, mà còn có vô vàn ứng dụng trong nhiều lĩnh vực khác nhau của đời sống và công nghiệp. Chúng ta hãy cùng điểm qua một số ứng dụng tiêu biểu của Ethanol nhé:
1. Đồ uống có cồn: “Linh hồn” của bia, rượu, và các loại đồ uống lên men
Ứng dụng quan trọng nhất và quen thuộc nhất của Ethanol chính là trong sản xuất đồ uống có cồn. Ethanol tạo ra vị cay nồng đặc trưng và tác động gây say khi uống các loại đồ uống này. Nồng độ Ethanol trong các loại đồ uống có cồn rất khác nhau:
- Bia: Thường có nồng độ cồn từ 3% đến 8%.
- Rượu vang: Thường có nồng độ cồn từ 8% đến 15%.
- Rượu mạnh (whisky, vodka, rum, tequila…): Thường có nồng độ cồn từ 40% trở lên.
2. Cồn sát khuẩn: “Vũ khí” chống lại vi khuẩn và virus
Ethanol với nồng độ 70% đến 75% là một chất sát khuẩn hiệu quả, được sử dụng rộng rãi trong y tế và đời sống hàng ngày để tiệt trùng da, dụng cụ y tế, và bề mặt. Cồn sát khuẩn giúp tiêu diệt vi khuẩn, virus, và nấm, ngăn ngừa nguy cơ nhiễm trùng và lây lan bệnh tật.
3. Nhiên liệu sinh học: “Xanh” và thân thiện với môi trường
Ethanol có thể được sử dụng làm nhiên liệu sinh học, thay thế cho xăng dầu truyền thống. Ethanol sinh học được sản xuất từ các nguồn nguyên liệu tái tạo như ngô, mía đường, cellulose thực vật, giúp giảm phát thải khí nhà kính và giảm sự phụ thuộc vào nhiên liệu hóa thạch. Ethanol sinh học có thể được sử dụng trực tiếp làm nhiên liệu cho động cơ đốt trong, hoặc pha trộn với xăng để tạo thành xăng sinh học (ví dụ xăng E5, E10).
4. Dung môi công nghiệp: “Trợ thủ đắc lực” trong sản xuất
Ethanol là một dung môi hữu cơ phổ biến, được sử dụng rộng rãi trong nhiều ngành công nghiệp:
- Công nghiệp hóa chất: Dung môi hòa tan, chất trung gian trong tổng hợp hóa học.
- Công nghiệp dược phẩm: Dung môi chiết xuất dược liệu, chất bảo quản trong một số loại thuốc.
- Công nghiệp mỹ phẩm: Dung môi trong nước hoa, kem dưỡng da, sản phẩm chăm sóc tóc.
- Công nghiệp thực phẩm: Dung môi chiết xuất hương liệu, chất bảo quản trong một số loại thực phẩm.
- Sản xuất sơn, mực in, chất tẩy rửa…
5. Ứng dụng khác: Vô vàn điều thú vị
Ngoài những ứng dụng chính trên, Ethanol còn có nhiều ứng dụng thú vị khác:
- Nhiệt kế rượu: Ethanol được sử dụng làm chất lỏng trong nhiệt kế rượu nhờ vào tính giãn nở vì nhiệt đều đặn và điểm đóng băng thấp.
- Chất chống đông: Ethanol có thể được sử dụng làm chất chống đông trong ô tô và các hệ thống làm lạnh ở vùng khí hậu lạnh.
- Bảo quản mẫu vật sinh học: Ethanol có thể được sử dụng để bảo quản mẫu vật sinh học nhờ vào khả năng khử nước và ngăn chặn sự phát triển của vi sinh vật.
- Trong phòng thí nghiệm: Ethanol được sử dụng làm dung môi, chất phản ứng, và chất làm lạnh trong nhiều thí nghiệm hóa học và sinh học.
Tác động của Ethanol đến cơ thể người: “Con dao hai lưỡi”
Ethanol có thể mang lại những trải nghiệm thú vị và lợi ích nhất định (như trong y tế, công nghiệp), nhưng cũng có thể gây ra những tác hại nghiêm trọng nếu sử dụng không đúng cách, đặc biệt là khi uống đồ uống có cồn. Chúng ta hãy cùng tìm hiểu về tác động của Ethanol đến cơ thể người nhé:
1. Tác động tích cực (khi sử dụng đúng mục đích và liều lượng)
- Sát khuẩn: Cồn sát khuẩn (Ethanol 70-75%) giúp tiêu diệt vi khuẩn, virus, ngăn ngừa nhiễm trùng.
- Giãn mạch máu: Một lượng nhỏ Ethanol có thể giúp giãn mạch máu, tăng cường lưu thông máu, và có thể có lợi cho tim mạch (tuy nhiên, lợi ích này còn gây tranh cãi và cần được nghiên cứu thêm).
- Giảm căng thẳng, thư giãn: Một lượng nhỏ Ethanol có thể giúp giảm căng thẳng, lo âu, và tạo cảm giác thư giãn, thoải mái (tuy nhiên, không nên lạm dụng để giải quyết vấn đề tâm lý).
2. Tác động tiêu cực (khi lạm dụng hoặc sử dụng không đúng cách)
- Gây say, ngộ độc: Uống quá nhiều đồ uống có cồn có thể gây say rượu, ngộ độc cồn, với các triệu chứng như mất kiểm soát vận động, buồn nôn, nôn mửa, đau đầu, chóng mặt, thậm chí hôn mê và tử vong.
- Gây hại cho gan: Gan là cơ quan chính chuyển hóa Ethanol. Uống quá nhiều rượu bia có thể gây ra các bệnh về gan như gan nhiễm mỡ, viêm gan do rượu, xơ gan, và ung thư gan.
- Gây hại cho hệ thần kinh: Ethanol có thể gây tổn thương não bộ, suy giảm trí nhớ, rối loạn giấc ngủ, rối loạn tâm thần, và nghiện rượu.
- Gây hại cho hệ tiêu hóa: Ethanol có thể gây viêm loét dạ dày – tá tràng, viêm tụy, rối loạn tiêu hóa, và tăng nguy cơ ung thư đường tiêu hóa.
- Gây hại cho tim mạch: Uống quá nhiều rượu bia có thể gây tăng huyết áp, rối loạn nhịp tim, suy tim, và bệnh cơ tim do rượu.
- Gây nghiện: Ethanol là chất gây nghiện. Nghiện rượu là một bệnh lý mãn tính nguy hiểm, gây ra nhiều hậu quả tiêu cực về sức khỏe, tinh thần, và xã hội.
- Ảnh hưởng đến thai nhi: Phụ nữ mang thai uống rượu bia có thể gây hại nghiêm trọng cho thai nhi, dẫn đến hội chứng nghiện rượu bào thai (FAS).
Lời khuyên: Sử dụng Ethanol đúng mục đích, đúng liều lượng, và có trách nhiệm. Đối với đồ uống có cồn, hãy uống có chừng mực, không lạm dụng, và tuyệt đối không lái xe sau khi uống rượu bia. Đối với cồn sát khuẩn, hãy sử dụng đúng nồng độ khuyến cáo và tránh tiếp xúc trực tiếp với mắt và niêm mạc.
Kết luận
Vậy là chúng ta đã cùng nhau khám phá thành phần chính của cồn – Ethanol, từ công thức hóa học, tính chất vật lý, hóa học, quy trình sản xuất, ứng dụng đa dạng, đến tác động của nó đối với cơ thể người. Hy vọng bài viết này đã giúp bạn hiểu rõ hơn về “linh hồn” của thức uống quen thuộc và những điều thú vị có thể bạn chưa biết về Ethanol.
Ethanol là một hợp chất hóa học đa năng, có vai trò quan trọng trong nhiều lĩnh vực của đời sống và công nghiệp. Tuy nhiên, cũng cần sử dụng Ethanol một cách có trách nhiệm để tận dụng những lợi ích và giảm thiểu tối đa những tác hại tiềm ẩn của nó.
Nếu bạn có bất kỳ câu hỏi hay muốn chia sẻ thêm về Ethanol, đừng ngần ngại để lại bình luận bên dưới để chúng ta cùng nhau trao đổi nhé! Chúc bạn luôn có những kiến thức bổ ích và thú vị!





